Melanoom
Behandeling
-
1. Uitzaaiing van melanoom voorkomen
2. Verdachte moedervlek: diagnostische excisie
3. Opvolging na behandeling van melanoom
4. Behandeling van een melanoom met uitzaaiingen
5. Behandelingen om de uitzaaiing of herval van een melanoom te voorkomen
1. Uitzaaiing van melanoom voorkomen
Als de schildwachtklier positief blijkt te zijn, en dus kankercellen bevat, is een tweede operatie nodig. Tijdens deze operatie zullen de andere regionale lymfeklieren (in de oksel, lies, hals) verwijderd worden. Dit is nodig omdat de kans bestaat dat ook in de aangrenzende lymfeklieren kankercellen zitten. Deze operatie noemen we een klieruitruiming.
Als uit de PET- of CT-scan is gebleken dat het melanoom zich heeft uitgezaaid in een of meer lymfeklieren, zal de chirurg meteen ook een klieruitruiming uitvoeren.
Een klieruitruiming kan soms complicaties teweegbrengen, zoals bewegingsbeperking, pijn, net zoals bij de okselklieruitruiming bij borstkanker. Sommige patiënten krijgen last van lymfoedeem: er ontstaat een zwelling die maanden of zelfs jaren na de operatie kan aanhouden. Dat komt omdat het lymfevocht zich ophoopt in een arm of been, nadat de lymfeklieren zijn verwijderd. Om die ophoping van vocht te verhelpen, kan men naar een kinesist gaan voor lymfedrainagetherapie.
Een adjuvante behandeling kan aangewezen zijn om het risico op herval, ook wel recidief genoemd, te beperken. Het woord 'adjuvant' betekent dat de patiënt in principe genezen is, maar dat hij toch nog een behandeling krijgt, zodat hij minder risico loopt op een recidief. Sommige patiënten met een melanoom lopen immers een hoog risico op een recidief. Dat zijn voornamelijk patiënten met tumorcellen in de lymfeklieren of patiënten bij wie het melanoom al uitgezaaid is naar andere plaatsen, maar bij wie de tumor volledig kon worden verwijderd. Tot voor kort werd alleen interferon overwogen als adjuvante behandeling van een melanoom. Tegenwoordig zijn er meerdere adjuvante behandelingsopties, zoals immunotherapie of doelgerichte therapie met Trametinib en Dabrafenib.
Artikel tot stand gekomen in samenwerking met dr. Isabelle Tromme, dermatoloog aan de Cliniques universitaires Saint-Luc.
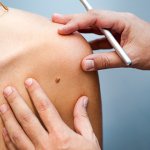
2. Verdachte moedervlek: diagnostische excisie
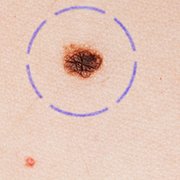
De diagnostische excisie
Als de dermatoloog vermoedt dat de verdachte pigmentvlek een melanoom zou kunnen zijn, zal hij direct proberen het deel van de huid waar het melanoom zich bevindt, te verwijderen. Deze procedure wordt de 'diagnostische excisie' genoemd, omdat ze tot doel heeft de tumor te verwijderen, maar ook na onderzoek de diagnose te stellen. Een excisie wordt uitgevoerd onder plaatselijke verdoving. Het weggenomen weefsel wordt ter analyse naar de anatoom-patholoog gezonden. Een moedervlek (verdacht of niet) mag nooit worden vernietigd, bv. met een laser, omdat het weefsel dan niet kan worden onderzocht. Gedeeltelijke verwijdering van de moedervlek door het bovenste deel eraf te schaven en het onderste deel ervan te verbranden (shave-coagulation genoemd), of door een gedeeltelijke biopsie, moet zo veel mogelijk worden vermeden. Deze technieken zijn soms noodzakelijk, maar worden slechts heel zelden uitgevoerd.
Chirurgische excisie
Als de patholoog-anatoom na analyse een melanoom diagnosticeert, moet een groter en dieper deel van het weefsel worden verwijderd.
Waarom wordt dat niet meteen gedaan bij de diagnostische excisie? Voordat hij een moedervlek en de huid eromheen wegneemt, wil de dermatoloog zeker weten dat het echt een melanoom is en niet een atypische moedervlek of een licht gepigmenteerde wrat. Bovendien is van tevoren niet duidelijk welke marges moeten worden aangehouden. De marge is de afstand tussen de tumor en de rand van het weggehaalde weefsel zonder kankercellen.
Tot slot is een al bestaand litteken van een grote excisie een nadeel wanneer nadien de schildwachtklier moet worden verwijderd.
Hoeveel huid moet worden verwijderd?
De excisiemarges hangen af van de dikte van het melanoom. Bij een melanoom in situ zijn de marges 0,5 cm. Bij een melanoom groter dan één centimeter in situ, wordt de Breslow-dikte bepaald. Als de Breslow-dikte twee millimeter of minder is, is een marge van 1 centimeter voldoende. Bij dikkere melanomen is de marge twee centimeter.
Bij de chirurgische excisie kan dus een grote wonde ontstaan, die niet kan worden gehecht. Om dergelijke wonden te sluiten maakt de chirurg gebruik van een transplantaat of huidflap. Dit betekent dat de chirurg een stukje huid zal nemen van een ander deel van het lichaam om de wonde te sluiten.
Artikel tot stand gekomen in samenwerking met dr. Isabelle Tromme, dermatoloog aan de Cliniques universitaires Saint-Luc.
3. Opvolging na behandeling van melanoom
Als het melanoom is behandeld, moeten de patiënten blijvend gecontroleerd worden.
- Bij elke patiënt die een melanoom heeft gehad, is er voor de rest van zijn leven nood aan een dermatologische nacontrole op regelmatige basis. Die controle dient om een tweede melanoom tijdig te kunnen opsporen. De patiënten wordt ook aangeraden zelf hun huid te controleren.
- Voor patiënten die een melanoom hebben gehad en een verhoogd risico hebben op herval/metastasen is ook een oncologische opvolging nodig. De frequentie van de bezoeken, het soort onderzoeken en de frequentie daarvan zijn afhankelijk van het risico op metastasen (d.w.z. de initiële Breslow-dikte), eventuele verzwering van het melanoom en aantasting van een of meer lymfeklieren.
Artikel tot stand gekomen in samenwerking met dr. Isabelle Tromme, dermatoloog aan de Cliniques universitaires Saint-Luc.
4. Behandeling van een melanoom met uitzaaiingen
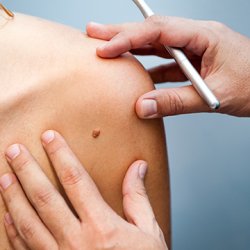
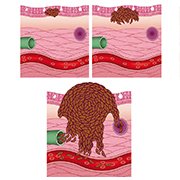
Als de kanker uitzaait …
De kankercellen kunnen in het bloed terechtkomen en vandaar andere plaatsen in het lichaam bereiken, met name de longen, de lever en de hersenen. Helaas is het bij de meeste patiënten met uitzaaiingen niet mogelijk om die uitzaaiingen te verwijderen, omdat ze te groot of onbereikbaar zijn.
Mogelijke behandelingen
Tot voor enkele jaren waren er weinig behandelopties voor een gemetastaseerd melanoom. Maar er is een grote doorbraak gekomen in het onderzoek en nu zijn er toch enkele doeltreffende behandelingen beschikbaar. Ondertussen kan men ook specifieke uitzaaiingen in de hersenen behandelen.
- Doelgerichte therapieën
- Immunotherapieën
Doelgerichte therapie in de kijker
Doelgerichte therapieën richten zich specifiek op bepaalde kankercellen. Zij herkennen deze kankercellen en remmen de processen af die ervoor zorgen dat de tumorcellen zich ongecontroleerd blijven vermenigvuldigen.
Doelgerichte therapieën bij melanoom richten zich op melanomen die een bepaalde genetische mutatie vertonen. Deze therapieën kunnen als monotherapie (één soort doelgerichte therapie) of als combinatietherapie (twee soorten doelgerichte therapieën tegelijkertijd) voorgeschreven worden.
BRAF-genmutatie begrijpen
Ongeveer 50% van de patiënten met een melanoom hebben een mutatie in het BRAF-gen.
Elke normale cel bevat een BRAF-eiwit dat de celgroei bepaalt. Dit gen wordt alleen geactiveerd bij celschade om de cel te herstellen. Bij sommige mensen is het BRAF-gen gemuteerd. Een verandering in het DNA veroorzaakt ongecontroleerde groei en celdeling, waardoor de tumor snel kan groeien.
BRAF-remmers en MEK-remmers worden gebruikt bij melanomen met een BRAF-mutatie gemetastaseerde setting (stadium IV irresectabel).
Hoe werkt doelgerichte therapie?
Doelgerichte therapieën blokkeren de BRAF- en MEK-eiwitten en verhinderen zo de groei en/of de verspreiding van kankercellen.
In normale omstandigheden werkt BRAF als een schakelaar die signalen doorgeeft om de
cellen in staat te stellen zich te ontwikkelen. Dat gebeurt alleen wanneer nodig. Op die manier wordt ongecontroleerde celgroei verhinderd.
Bij patiënten die BRAF-positief zijn, blijf het eiwit constant 'aan'. Dat leidt tot continue signalen die een ongecontroleerde celgroei uitlokken. Het doel van de behandeling is om de BRAF-MEK-eiwitten te blokkeren, zodat de tumorcellen afsterven.
Welke doelgerichte therapie bestaat er voor huidkanker?
Er bestaan momenteel vier geneesmiddelen voor de doelgerichte therapie van BRAF-positieve huidkanker.
De eerste doelgerichte behandeling omvatte Dabrafenib, de eerste doelgerichte remmer van het BRAF-eiwit, en Trametinib, dat het MEK-eiwit afremt.
Dabrafenib kan afzonderlijk gegeven worden, maar wordt bijna altijd in combinatie met Trametinib gegeven, omdat de werking van de twee geneesmiddelen samen doeltreffender is.
Enkele jaren later kwamen Braftovi, dat het RAF-eiwit remt, en Mektovi, dat het MEK-eiwit remt, op de markt. Braftovi en Mektovi worden momenteel enkel terugbetaald voor de behandeling van gemetastaseerd melanoom, terwijl Dabrafenib en Trametinib zowel voor adjuvant als gemetastaseerd melanoom worden terugbetaald.
Voordelen van doelgerichte therapie
Alle doelgerichte therapieën die momenteel gegeven kunnen worden voor de behandeling van melanoom zijn oraal, ze bestaan in pil- of capsulevorm en worden ingenomen met water. Het grote voordeel hiervan is dat de patiënt niet naar het ziekenhuis hoeft te komen voor zijn behandeling.
Zoals bij elke behandeling kan men als patiënt nevenwerkingen ervaren. De meest frequente nevenwerkingen van doelgerichte therapieën zijn koorts en gastro-intestinale ongemakken. Deze nevenwerkingen zijn reversibel, wat betekent dat ze weggaan als de dosis aangepast wordt of de behandeling stopgezet wordt.
Immunotherapie in de kijker
Immuuntherapie, ook wel biologische geneesmiddelen (of monoklonale antilichamen) genoemd, stimuleert het immuunsysteem om kanker te helpen bestrijden.
Immunotherapie kan in monotherapie (één soort immuuntherapie) of in combinatietherapie (twee soorten immuuntherapie) gegeven worden.
Immunotherapie: hoe werkt het?
Immunotherapie is een kankerbehandeling waarbij het immuunsysteem (afweersysteem) van de patiënt wordt gestimuleerd, met als doel de kankercellen te bestrijden en te vernietigen. Het is dus niet de behandeling zelf die de kankercellen vernietigt. De behandeling mobiliseert het immuunsysteem – vooral bepaalde witte bloedcellen zoals de T-lymfocyten – om de kanker ‘op natuurlijke wijze’ te vernietigen.
Welke immunotherapie bestaat er voor huidkanker?
Er bestaan momenteel drie soorten immunotherapie voor de behandeling van huidkanker:
Nivolumab: een monoklonale antistof die zicht focust op de PD-1-receptor die aanwezig is in de T-lymfocyten; Pembrolizumab, een monoklonale antistof die zich focust op de PD-1-receptor die aanwezig is in de T-lymfocyten; en Ipilumumab, een molecule die zich op de CTLA-4-recepter focust.
Nivolumab kan afzonderlijk of in combinatie met Ipilumumab toegediend worden, afhankelijk van het ziektestadium.
Pembrolizumab kan enkel afzonderlijk toegediend worden.
Voordelen van immunotherapie
Immunotherapie wordt toegediend via een infuus en kan worden gebruikt bij elk soort melanoom, ongeacht of het een genetische mutatie heeft.
Zoals bij elke behandeling kan men als patiënt nevenwerkingen ervaren. Bij immunotherapieën ligt het aandeel patiënten die nevenwerkingen ervaren vrij laag.
De meest frequente nevenwerkingen van immunotherapie zijn een verlaagd aantal witte bloedcellen, die instaan voor de afweer, en gastro-intestinale ongemakken. Aan de andere kant zijn er ook patiënten (een kwart) bij wie het immuunsysteem te extreem reageert op de behandeling. Wanneer dat gebeurt, valt het immuunsysteem de gezonde cellen aan. De nevenwerkingen die gelinkt zijn aan het immuunsysteem zijn irreversibel, wat betekent dat ze niet meer weggaan.
Artikel tot stand gekomen in samenwerking met dr. Isabelle Tromme, dermatoloog aan de Cliniques universitaires Saint-Luc.
5. Behandelingen om de uitzaaiing of herval van een melanoom te voorkomen

-
Doelgerichte therapieën
Doelgerichte therapieën richten zich specifiek op bepaalde kankercellen. Zij herkennen de kankercellen en remmen de processen af die ervoor zorgen dat de tumorcellen zich ongecontroleerd blijven vermenigvuldigen.Doelgerichte therapieën bij melanoom richten zich op melanomen die een bepaalde genetische mutatie vertonen. Deze therapieën kunnen als monotherapie (één soort doelgerichte therapie) of als combinatietherapie (twee soorten doelgerichte therapieën tegelijkertijd) voorgeschreven wordenOngeveer 50% van de patiënten met een melanoom hebben een mutatie in het BRAF-gen. Elke normale cel bevat een BRAF-eiwit dat de celgroei bepaalt. Dit gen wordt alleen geactiveerd bij celschade om de cel te herstellen. Bij sommige mensen is het BRAF-gen gemuteerd. Een verandering in het DNA veroorzaakt ongecontroleerde groei en celdeling, waardoor de tumor snel kan groeien.
Dabrafenib en Trametinib zijn momenteel de enige terugbetaalde BRAF-remmers en MEK-remmers die mogen worden gebruikt voor de behandeling van adjuvant melanoom.
Dabrafenib en Trametinib zijn orale therapieën, dit wil zeggen dat het medicijn in pil- of capsulevorm in te nemen is met water. Het grote voordeel hiervan is dat de patiënt niet naar het ziekenhuis hoeft te komen voor zijn behandeling.
Zoals bij elke behandeling kan men als patiënt nevenwerkingen ervaren. De meest frequente nevenwerkingen van doelgerichte therapieën zijn koorts en gastro-intestinale ongemakken. Die nevenwerkingen zijn reversibel, wat betekent dat ze verdwijnen als de dosis aangepast wordt of de behandeling stopgezet wordt.
-
Immunotherapieën
Immuuntherapie, ook wel biologische geneesmiddelen (of monoklonale antilichamen) genoemd, stimuleren het immuunsysteem om kanker te helpen bestrijden.Immunotherapie voor de behandeling van adjuvant melanoom is enkel goedgekeurd in monotherapie (één soort immuuntherapie) voor Pembrolizumab en Nivolumab.
Immunotherapie wordt toegediend via een infuus en kan worden gebruikt bij elk soort melanoom, ongeacht of het een genetische mutatie heeft.
Zoals bij elke behandeling kan men als patiënt nevenwerkingen ervaren. De meest frequente nevenwerkingen van immunotherapie zijn een verlaagd aantal witte bloedcellen, die instaan voor de afweer, en gastro-intestinale ongemakken. Aan de andere kant zijn er ook patiënten (een kwart) bij wie het immuunsysteem te extreem reageert op de behandeling. Wanneer dat gebeurt, valt het immuunsysteem de gezonde cellen aan. Nevenwerkingen die gelinkt zijn aan het immuunsysteem zijn irreversibel, wat betekent dat ze niet meer weg zullen gaan.
Artikel tot stand gekomen in samenwerking met dr. Isabelle Tromme, dermatoloog aan de Cliniques universitaires Saint-Luc.
NIEUWS
 27 04 2026
27 04 2026
Melanoom
Gebronsde huid, onzichtbare risico’s
Huidkanker blijft de maligniteit waarvan de incidentie in België het snelst toeneemt, met een spectaculaire stijging van het aantal gevallen in de voorbije twintig jaar....
Lees verder 15 01 2024
15 01 2024
Melanoom
Huidkankervaccins al in 2025 verkrijgbaar?
Farmabedrijf Moderna hoopt in 2025 een huidkankervaccin in de markt te zetten. “De resultaten zijn echt veelbelovend”, zegt Evelien Smits, professor kankerimmuuntherapie...
Lees verder 23 10 2023
23 10 2023
Borstkanker
"Stop met te zeggen dat je moet vechten tegen kanker"
"Laat dat vechten over aan dokters en onderzoekers. Patiënten hebben vooral steun en troost nodig”, aldus de hoofdredacteur op VRT NWS. "Vechten tegen kanker, het is ook...
Lees verder 23 10 2023
23 10 2023
Melanoom
“Tegen 2030 kunnen de eerste kankervaccins er zijn”
De mRNA-technologie... Een baanbrekend stukje technologie, dat volgens Klinisch biologe Isabel Reloux-Roels (UZ Gent) bij eventuele toekomstige pandemieën opnieuw kan ing...
Lees verderUW FAVORIETE ITEMS
 10 01 2024
10 01 2024
Melanoom
Immunotherapie beter laten aanslaan bij melanoom
Door een specifiek type melanoomcellen in het vizier te nemen, kan de reactie op immunotherapie verbeteren.
Melanoom: de doeltreffendheid van immunotherapie sterk te ve
... Lees verderKORT
OPINIEPEILING
GETUIGENISSEN
“Er is op korte tijd veel vooruitgang geboekt”

Dr. Annemie Rutten, Afdelingshoofd Medische oncologie, GZA
Melanoom: uitgestelde opsporing door COVID-19

Dr. Nathalie Rooseleer, vrijwillige dermatoloog verbonden aan het taskforce van Euromelanoma België
TEST JEZELF
ZIEKTES IN DE KIJKER
Alzheimer
Chronische myeloïde leukemie
Covid-19
Migraine en hoofdpijn
Oogontsteking, oogirritatie of droge ogen
Overactieve blaas
Parkinson
Transplantatie van organen
PREVENTIE IN DE KIJKER
Alle thema'sNEWSLETTER
IN FOTO