Insuffisance rénale
-
1. 10 infos pour mieux les connaître les reins
2. Allo maman, mes reins sont malades!
3. Analgésiques: quels sont les risques pour les reins?
4. Anémie et insuffisance rénale: quelles solutions?
5. Apnée du sommeil: un danger pour le coeur?
6. Assurances: ne vous laissez pas faire!
7. Au secours! Des kystes envahissent mes reins!
8. Biopsie rénale: avant, pendant et après
9. Calculs rénaux: les reins en danger
10. Ces jambes qui ne trouvent jamais le repos...
11. Cola et rein: une liaison dangereuse?
12. Comment rendre la dialyse plus agréable?
13. Cystinose: mieux la comprendre pour mieux la traiter
14. Dépistage de l'insuffisance rénale
15. Des pieds sous haute protection
1. 10 infos pour mieux les connaître les reins
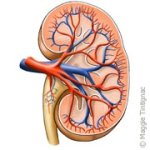
1. Nous avons tous 2 reins ; ils pèsent chacun 160 grammes et mesurent environ 12 cm de long et 6 cm de large.
2. Un rein est capable d’effectuer le travail des 2 reins. Notre réserve fonctionnelle rénale est donc grande.
3. Les reins se situent dans la partie supérieure de l'abdomen, de part et d'autre de la colonne vertébrale. Ils sont entourés d'un coussinet de graisse protectrice.
4. Pour localiser les reins, il suffit de poser ses mains sur ses hanches et de les diriger vers le haut jusqu’aux côtes, puis de placer ses pouces contre le dos : les reins situent juste en dessous !
5. Les reins purifient jusqu'à 170 litres de sang par jour.
6. Les reins éliminent les déchets du sang (eau et sel en excès). Plus de 1,5 litres d’urine sont produits et acheminés chaque jour des reins vers la vessie, soit quelques millilitres toutes les 10 à 15 secondes.
7. Chaque rein est composé d'environ 1 million de néphrons. Chaque néphron comporte un glomérule (filtre qui laisse passer l'eau et les déchets contenus dans le sang mais retient les grosses molécules telles que les protéines et les globules rouges) et un tubule (filtre indispensable à la formation de l'urine définitive).
8. Dans 100 grammes d’urine, 96 grammes se composent d'eau; le reste est constitué de sels minéraux et de déchets riches en azote.
9. Assurant la filtration du sang et la production d'urine, les reins fabriquent aussi plusieurs hormones : l’érythropoïétine (EPO), qui stimule la moëlle osseuse à produire des globules rouges; la rénine, impliquée dans le contrôle de la tension artérielle; le calcium et la vitamine D, qui interviennent dans le métabolisme osseux.
10. Les reins équilibrent également la teneur en eau de notre corps. Comme la quantité d'eau contenue dans notre organisme dépend de la quantité de sel qui s'y trouve, les reins doivent veiller à ce que la quantité de sel éliminée dans les urines corresponde à la quantité de sel apportée par l'alimentation.
Pour plus d'infos sur la journée mondiale du rein:http://www.worldkidneyday.org.
2. Allo maman, mes reins sont malades!
Avant la naissance ou durant l'enfance
"70% des enfants atteints d'insuffisance rénale sont touchés par cette pathologie dès la naissance," explique le Pr Françoise Janssen, chef de clinique du service de néphrologie de l'hôpital Universitaire des Enfants Reine Fabiola. "Parmi eux, certains souffrent d'une maladie génétique héréditaire, d'autres d'une malformation des voies urinaires ou d'un développement anormal des reins pouvant apparaître dès les premiers jours après la naissance. Les maladies rénales dites acquises concernent quant à elles environ 30 % des enfants."
Dépistage chez le foetus
Par le biais d'échographies effectuées avant la naissance et/ou d'un dépistage génétique, il est possible de repérer très tôt les malformations congénitales ou héréditaires pouvant être à l'origine d'une insuffisance rénale. Comme le précise le Pr Janssen, "lorsque la maladie est identifiée, une interruption de grossesse est proposée aux parents. Certaines malformations (reins trop petits ou présentant un nombre insuffisant de filtres rénaux) ne peuvent toutefois pas toujours être diagnostiquées." La prise en charge de l'enfant par une équipe multidisciplinaire composée notamment de pédiatres, de chirurgiens pédiatriques, de néphrologues, de diététiciens et d'infirmiers s'avère dès lors indispensable pour ralentir la progression de l'insuffisance rénale.
Les modalités du traitement
"Dans la plupart des cas, l'évolution de l'insuffisance rénale se révèle assez lente. Un traitement dit "conservateur" peut donc être prescrit pendant de nombreuses années", souligne la spécialiste. Comme pour les adultes, un régime pauvre en protéines, en potassium, en phosphore et en sodium doit être suivi. Outre de l'érythropoïétine (substance corrigeant l'anémie), des médicaments chargés de rétablir l'équilibre de l'organisme et des suppléments de vitamine D, les enfants reçoivent également des injections sous-cutanées d'hormone de croissance avec comme objectif de leur permettre de se maintenir à un poids et une taille normale malgré leur maladie.
La greffe, une étape salutaire
Les enfants qui souffrent d'une néphropathie héréditaire sont parfois suivis durant une vingtaine d'années sans devoir passer par la dialyse. Lorsque l'insuffisance rénale atteint le stade terminal, l'idéal serait dès lors de pouvoir recourir directement à la greffe sans devoir passer par la case "dialyse". "De nombreux parents se portent volontaires au don de rein, se réjouit le Pr Janssen. Malheureusement, tous n'appartiennent pas à un groupe tissulaire compatible à celui de leur enfant… En Belgique, pays faisant partie d'Eurotransplant (1), les jeunes patients n'ont que quelques points de priorité par rapport aux adultes sur la liste d'attente pour une greffe. Il arrive donc souvent que certains soient pris en charge en dialyse plus d'un an avant de pouvoir être transplantés."
Aurélie Bastin, avec la collaboration du Pr Janssen, chef de clinique du service de néphrologie de l'hôpital Universitaire des Enfants Reine Fabiola.
(1) Organisme international regroupant les centres de transplantation de six pays : Allemagne, Autriche, Belgique, Luxembourg, Pays-Bas et Slovénie.
3. Analgésiques: quels sont les risques pour les reins?
"Les patients atteints d’un déficit de la fonction rénale doivent faire preuve d’une grande prudence lorsqu’ils prennent un médicament de manière prolongée, quel qu’il soit. Un suivi régulier de la fonction rénale et de la quantité de calcium et de phosphate présente dans l'organisme est, dans ce cas, plus que jamais indispensable », précise d'emblée le Pr Vanrenterghem. La prise d'anti-inflammatoires non stéroïdiens (AINS) peut en effet s’accompagner d’une altération temporaire de la fonction rénale, même si elle n'est qu’exceptionnellement à l’origine d'une insuffisance rénale.
Anti-inflammatoires: attention danger!
La prise d'un seul comprimé d'AINS peut toutefois provoquer une légère diminution de la fonction rénale. Généralement temporaire, cette altération disparaît dès l’arrêt du traitement. Pour les patients âgés atteints d’affections rhumatismales, telles que l’arthrite ou l’arthrose, et qui suivent des traitements anti-inflammatoires prolongés, le risque de dégradation de la fonction rénale est beaucoup plus important. Les patients qui présentent une fonction rénale déjà déficiente et qui consomment ces médicaments risquent quant à eux d'aggraver encore davantage leur maladie. En cause: la réduction de l'irrigation sanguine provoquée par ces molécules au niveau rénal. Ajoutons enfin que l'association d'AINS avec une légère déshydratation ou avec la prise de médicaments inhibiteurs de l'enzyme de conversion de l'angiotensine (traitement de l'hypertension artérielle notamment) peut également accentuer de manière dramatique les risques de dégradation de la fonction rénale.
Le paracétamol: inoffensif
Par le passé, de nombreux cas d’insuffisance rénale étaient dus à un usage excessif, voire abusif, de médicaments antidouleur contenant de la phénacétine. « Il y a quinze ans, la moitié des patients admis dans notre centre de dialyse avait pris ces médicaments en trop grande quantité", confirme le Pr Vanrenterghem. Cette substance est aujourd'hui retirée du marché. Quant au paracétamol (le principe actif de médicaments antidouleur tels que le Dafalgan), aucune étude ne permet de mettre en évidence qu'il entraînerait un quelconque effet nocif sur les reins. Les soupçons qui pesaient autrefois sur cette substance devaient probablement provenir du fait que certains médicaments antidouleur contenaient de la phénacétine associée au paracétamol. Aujourd’hui, le paracétamol est en vente libre et considéré comme absolument inoffensif pour les reins.
Guy Bourgeois, avec la collaboration du Pr Yves Vanrenterghem, chef du service de néphrologie au Centre Hospitalier Universitaire Leuven-Gasthuisberg.
4. Anémie et insuffisance rénale: quelles solutions?
Dans le sang, le transport de l'oxygène est assuré par l'hémoglobine, une protéine présente dans les globules rouges. En cas d'anémie, le nombre de globules rouges dans le sang diminue, ce qui entraîne une moins grande capacité du sang à transporter l'oxygène vers les organes et les muscles. Cette pathologie est très souvent associée à l'insuffisance rénale. Les reins ont en effet pour mission de produire une hormone, l'érythropoïétine (ou EPO), qui stimule la production des globules rouges et donc de l'hémoglobine. Quand la fonction rénale diminue, notre organisme produit donc de moins en moins d'EPO, et l'anémie se met en place petit à petit, très discrètement.
Difficile à supporter
La fatigue intense, les troubles de la concentration et du sommeil, et le manque d'énergie accompagnent souvent le quotidien des patients souffrant d'anémie. Cette complication n'est donc pas seulement une conséquence très fréquente de l'insuffisancerénale, elle est aussi l'une des plus difficiles à supporter. En l'absence de prise en charge adéquate, l'anémie influence directement l'activité cardiaque. Comme le sang transporte moins d'oxygène, le c'ur doit battre plus vite. Les patients risquent alors de développer une hypertrophie ventriculaire gauche, complication qui augmente le risque de mortalité par accident cardiaque.
Un traitement révolutionnaire
Depuis plus de 15 ans, les médecins utilisent un traitement médicamenteux pour élever le taux d'EPO des patients anémiés. Son apparition a constitué un grand progrès pour les personnes souffrant d'anémie. "La qualité de vie des malades s'améliore très grandement dès la délivrance du médicament" témoigne le Pr Krzesinski, chef du service de néphrologie du Centre Hospitalier Universitaire de Liège. "Par ailleurs, d'après mon expérience, les patients dont l'anémie est traitée tôt supportent plus facilement l'insuffisancerénale. Ce traitement semble également permettre une mise sous dialyse plus tardive." Les traitements stimulant la production de globules rouges ne constituent cependant pas la réponse unique et automatique à toutes les anémies: il n'est pas efficace en cas de manque de fer, ou si l'anémie est causée par une déficience en vitamine B 12 ou en acide folique. Par ailleurs, d'autres maladies que l'insuffisancerénale peuvent déclencher une anémie. Leur présence doit donc être éliminée avant de mettre en place ce type de traitement.
Le bon dosage
Même lorsqu'il est approprié, ce type de traitement par agents stimulateurs de l'EPO n'est pas sans risque. Une augmentation trop rapide de l'hémoglobine dans le sang peut entraîner des effets indésirables: hypertension, risque de thromboses... Le traitement doit donc viser une augmentation douce de l'EPO (pas plus d'un gramme par litre de sang en plus par mois, d'après le Pr Krzesinski) et tendre à rejoindre la norme plutôt qu'à la dépasser.
Marion Garteiser
5. Apnée du sommeil: un danger pour le coeur?

Selon une étude parue en novembre 2009 dans le Clinical Journal of the American Society of Nephrology, l'apnée du sommeil serait associée à un risque accru d'hypertension artérielle, de maladie cardiovasculaire et de crise cardiaque chez les insuffisants rénaux en attente de greffe ou ayant subi une greffe de rein.
Mauvais contrôle de l'hypertension
Les chercheurs ont étudié plus de 100 personnes greffées du rein et 50 personnes en attente de greffe. Résultat: un patient sur quatre présente de nombreuses apnées durant son sommeil. Les chercheurs ont également constaté que plus de la moitié des personnes greffées souffrant d'apnée du sommeil doivent être traitées avec plus de trois médicaments pour réduire leur hypertension. Malgré ces traitements, leur pression sanguine reste beaucoup plus élevée par rapport aux patients qui ne souffrent pas d'apnée du sommeil.
Plus de maladies cardiovasculaires
Selon les chercheurs, l'augmentation de la pression sanguine due aux apnées du sommeil chez les patients dialysés ou greffés contribuerait au développement de maladies cardiovasculaires. Ces derniers auraient ainsi deux fois plus de risques de développer des maladies cardiovasculaires ou de subir une crise cardiaque que les patients qui ne souffrent pas d'apnée.
Prévenir les apnées du sommeil
De nombreux patients ignorent qu'ils sont sujets aux apnées du sommeil. Les médecins doivent donc être attentifs à ce problème. Le cas échéant, un traitement peut en effet être proposé.
Source: "Sleep Apnea Is Associated with Cardiovascular Risk Factors among Kidney Transplant Patients", appeared online at http://cjasn.asnjournals.org/ on Thursday, November 19, 2009, doi 10.2215/CJN.04030609.
6. Assurances: ne vous laissez pas faire!

Ne mentez pas!
Vu les difficultés qu'il y a à se faire assurer quand on est atteint d'une maladie grave et/ou chronique, la tentation est grande de mentir ou d'omettre certaines informations importantes. Mauvaise idée! Car si l'assureur parvient à prouver votre fraude, il peut refuser d'intervenir le jour où vous en aurez besoin. Son "droit de savoir" n'est toutefois pas absolu. La loi vous oblige à lui fournir toute information lui permettant d'évaluer le risque pour lequel vous demandez une couverture. Les données génétiques (antécédents familiaux) et les spéculations quant à l'évolution future de votre état de santé ne peuvent en aucun cas être communiquées. Si de telles questions vous sont posées, vous n'avez pas à y répondre.
Méfiez-vous des médecins-conseils
Avant, pendant ou après la conclusion du contrat d'assurance, l'assureur peut exiger que vous soyez examiné par un de ses médecins-conseils. Trois choses à savoir à son sujet:
1) L'avis du médecin-conseil conditionne très souvent la décision de l'assureur.
2) Étant rémunéré par l'assureur, le médecin-conseil est davantage de son côté que du vôtre.
3) Après vous avoir vu, le médecin-conseil rédige un rapport qu'il envoie à l'assureur. En vertu de la loi sur les droits des patients, vous pouvez (et devez!) exiger une copie de ce rapport pour pouvoir, le cas échéant, le compléter, voire le contester.
Payez à temps
À moins que certaines clauses dans le contrat ne l'y autorisent ou que vous ayez commis une fraude (un mensonge, par exemple), l'assureur n'a pas le droit de modifier ou d'annuler un contrat d'assurance-vie ou maladie en cours. Mais dans les faits, certaines compagnies moins scrupuleuses peuvent profiter d'un défaut ou d'un retard de paiement pour "annuler" votre assurance. Veillez donc à toujours payer vos primes à temps et à être en ordre.
Vous n'êtes pas seul...
Face aux assurances, vous êtes un peu David contre Goliath. Heureusement, certains organismes peuvent vous aider:
- L'Ombudsman des assurances (www.ombudsman.as) recueille gratuitement les plaintes relatives à un contrat d'assurance. Ce médiateur tente de trouver une solution à l'amiable entre l'assuré et l'assureur.
- Si vous pensez être victime d'une discrimination injustifiée, le Centre pour l'égalité des chances (www.diversite.be) est compétent pour recueillir votre plainte.
- Les associations de patients et/ou de défense des consommateurs peuvent soutenir des actions en justice menées en votre nom. N'hésitez pas à prendre contact avec elles.
Article réalisé avec la collaboration du Pr Hubert Claassens, professeur de droit émérite à la KUL.
7. Au secours! Des kystes envahissent mes reins!
Se manifestant souvent par de l’hypertension, des douleurs lombaires, du sang dans les urines, voire des infections ou des calculs rénaux, cette maladie rénale peut aussi être asymptomatique et découverte à l’occasion d’une échographie abdominale. "Lorsque le diagnostic est posé chez un patient, un dépistage par échographie peut être proposé aux membres de sa famille", explique le Dr Frédéric Debelle, chef de clinique adjoint au service de néphrologie de l'hôpital Erasme. A ce stade, les kystes sont déjà visibles, mais la maladie n'est généralement pas suffisamment évoluée que pour nécessiter un traitement par dialyse. L'appui d'un généticien et d'un néphrologue est toutefois souhaitable. "Il faut pouvoir rassurer le patient et lui expliquer clairement de quoi il souffre et quelles seront les conséquences de sa maladie aussi bien pour lui que pour ses éventuels descendants", poursuit le spécialiste.
Progression aléatoire
D'autant que la polykystose peut évoluer de manière extrêmement variable d'une personne à l'autre. "Au fil du temps, en devenant de plus en plus nombreux et de plus en plus volumineux, les kystes finissent par abîmer le rein." Une dégradation qui est en général très lente, mais qui peut parfois ne prendre que quelques années. "Un certain nombre de patients, fort heureusement limité (moins de 2%), sont déjà sous dialyse avant l'âge de 40 ans alors que d'autres conservent encore une fonction rénale suffisante à 70 ans", souligne le Dr Debelle.
Précision importante: rien ne sert de s'affoler lorsqu'un ou deux kystes seulement sont détectés. "Outre certaines maladies rares, l'âge peut favoriser l'apparition de kystesrénaux sans aucun lien avec la polykystose. D'après les estimations, de 4 à 5 % de la population âgée de 50 à 70 ans seraient porteurs de tels kystes." Il faut également savoir que les maladies rénales, quelles qu'elles soient, peuvent elles aussi favoriser l'apparition de kystes sans lien avec la maladie génétique.
Un vent d'espoir…
Aucun médicament spécifique n'étant disponible à ce jour, le traitement de la polykystose est identique à celui des autres maladies rénales. La seule différence se marque au stade de la préparation à la greffe. "Les reins kystiques peuvent être particulièrement volumineux et compromettre sérieusement la mise en place du futur greffon. Dans ce cas, mais également en cas de douleurs, saignements et/ou infections répétés des kystes, une néphrectomie (ablation d’un, voire des 2 reins) peut être envisagée avant que le patient soit inscrit sur la liste d'attente pour une greffe", souligne le Dr Debelle. Autre particularité: la polykystose étant une maladie héréditaire, un examen approfondi doit être réalisé lorsqu'un membre de la famille souhaite faire don de l'un de ses reins au patient.
Notons enfin qu'une nouvelle classe de médicaments, les antagonistes des récepteurs à la vasopressine, pourrait être capable de freiner l'évolution des kystes et donc ralentir la progression de l’insuffisancerénale. En cours d'évaluation chez les patients, ce traitement pourrait être disponible dans les prochaines années.
Aurélie Bastin, avec la collaboration du Dr Frédéric Debelle, chef de clinique adjoint au service de néphrologie de l'hôpital Erasme.
8. Biopsie rénale: avant, pendant et après
Une biopsie rénale est un examen qui consiste à prélever un ou plusieurs fragments de rein (en général deux ou trois) de la taille d'un quart d'allumette. Le prélèvement est ensuite examiné au microscope, de manière à pouvoir établir un diagnostic de maladie rénale.
Dans quels cas est-il pratiqué?
• Présence de protéine (albumine ou autre) et/ou de sang dans les urines.
• Insuffisance rénale aiguë (altération brutale de la fonction rénale sans cause évidente) ou chronique.
• Pathologies systémiques comme le lupus.
• Détérioration de la fonction rénale après une greffe rénale (risque de rejet).
Comment se déroule l'examen?
Il faut tout d'abord arrêter la prise de médicaments anticoagulants (quelques jours avant la biopsie) et la prise d'antiagrégants plaquettaires comme l'aspirine (une dizaine de jour avant). Quelques heures avant l'examen, un bilan de coagulation est réalisé. Lorsque les résultats de la prise de sang sont connus, la biopsie peut commencer. Un examen échographique est d’abord réalisé afin de déterminer lequel des reins est le plus accessible et de contrôler qu'il n'existe pas de contre-indication à la biopsie (dilatation des cavités du rein par exemple). Le médecin réalise ensuite une anesthésie locale dans le bas du dos. Une fine aiguille est alors introduite dans le rein afin de prélever les fragments qui seront analysés. Grâce à l'anesthésie locale, cet examen n'est pas douloureux.
Après la biopsie
Le patient reçoit ensuite une perfusion d'hydratation (liquide physiologique) jusqu'à ce qu'il urine. Si les urines sont claires, il peut boire, manger et se lever. Si du sang passe dans ses urines, il doit attendre les suivantes pour s'assurer qu'elles s'éclaircissent. Il peut ensuite rejoindre son domicile. Si le patient est arrivé le matin, il peut donc généralement repartir en fin de journée. Dans la semaine qui suit l'examen, le patient devra s'abstenir de faire des efforts violents pour éviter de solliciter les muscles lombaires, au risque de créer un petit hématome musculaire.
Les complications éventuelles
Il est possible que du sang soit présent dans les urines après biopsie: en trop grande quantité, celui-ci peut amener à la formation de caillots bloquant le passage de l'urine. Dans ce cas, il est nécessaire de poser une sonde pour éviter l'accumulation d'urine dans la vessie. Des hématomes autour du rein ou dans les muscles lombaires consécutifs au prélèvement peuvent aussi apparaître mais ils sont généralement sans conséquence.
La complication la plus sérieuse est l'apparition d'une fistule urinaire, c'est-à-dire d'une communication anormale entre une artère du rein (accidentellement blessée par l'aiguille lors du prélèvement) et les cavités du rein. Très rare, cette complication peut nécessiter une intervention chirurgicale afin d'arrêter l'hémorragie consécutive à la fistule.
Julie Luong, avec la collaboration du Dr Christophe Bovy, néphrologue au Centre Hospitalier Universitaire de Liège.
9. Calculs rénaux: les reins en danger

Selon les statistiques, 5 à 10% de personnes souffriront au moins une fois au cours de leur vie de calculs rénaux, plus communément appelés "pierres aux reins". Ces petites pierres de dimensions variables se forment au niveau du rein suite à la cristallisation d'un excès de substances minérales présentes normalement dans l'urine. Les calculs s'éliminent en principe spontanément. Il arrive toutefois qu'un calcul se bloque dans l'urètre, le canal qui relie le rein à la vessie, ce qui provoque de vives douleurs dans le bas du dos.
Un risque plus élevé de maladie rénale
Selon une étude présentée lors du 41e congrès de la société de néphrologie américaine, les calculs rénaux augmentent de 60% le risque de maladie rénale chronique. Le risque de développer une insuffisance rénale terminale est quant à lui augmenté de 40%. Les patients doivent dans ce cas être traités par dialyse ou nécessitent une transplantation.
Le calcul rénal: cause ou conséquence?
Selon le Dr Agnieszka Pozdzik, néphrologue à l'Hôpital Erasme à Bruxelles, "il y a un lien étroit entre calcul rénal et maladie rénale. Suivant sa taille, le calcul peut en effet bloquer les voies urinaires basses et être responsable d'une insuffisance rénale aiguë. Le calcul peut également être le signe d'un désordre métabolique. Il peut révéler une maladie rénale existante d'origine génétique, une malformation des reins ou des voies urinaires, voire même une maladie prédisposant à la formation de calculs." Ceux-ci ne doivent donc pas être pris à la légère.
Prise en charge multidisciplinaire des patients
Un diagnostic tardif ou erroné, un traitement inadapté ou insuffisant, sont des facteurs qui contribuent au développement d'une insuffisance rénale chronique chez les patients présentant des calculs rénaux. Une prise en charge pluridisciplinaire et un contrôle régulier de la fonction rénale permettent de limiter le risque d'insuffisance rénale chez ces patients et, indirectement, de diminuer le risque de récidive de calculs rénaux.
10. Ces jambes qui ne trouvent jamais le repos...
1h20, Paula ferme finalement les yeux. Sortie de dialyse à 19h, vidée, épuisée, elle essayait de s'endormir depuis des heures. 3h30, ses jambes se réveillent.… Elle ouvre à nouveau les yeux. Atteinte d'insuffisance rénale chronique depuis 10 ans, Paula souffre également du syndrome des jambes sans repos (SJSR). Un nom plutôt poétique pour une réalité qui l'est beaucoup moins. Alors que le soleil se couche, lorsqu'elle est prête à s'endormir, Paula est en prise à d'intenses fourmillements dans les jambes. Impossible de rester couchée! Seule la marche libère Paula de cette sensation étrange et indescriptible, entre picotement, douleur et inconfort.
Un mal encore très mystérieux
"S'il est avéré que le syndrome des jambes sans repos correspond à un trouble du système nerveux, le mécanisme biochimique qui entraîne ces impatiences reste encore en grande partie mystérieux", reconnaît le Pr Vandervelde, chef du service de néphrologie des hôpitaux Iris Sud. "Au sein d'une même famille, plusieurs personnes en sont souvent atteintes. L'existence d'une composante génétique de ce syndrome n'est donc pas à exclure." Dans plus de 40 % des cas, le SJSR est dit "primaire", ce qui signifie qu'aucune cause précise ne peut lui être associée. Dans les autres cas, le SJSR est dit "secondaire". Le manque de fer ou la prise de médicaments (antidépresseurs, tranquillisants, anti-nauséeux…) sont en effet quelques-uns des facteurs pouvant favoriser l'apparition de ce syndrome. Signe de la détérioration de la fonction rénale, l'urémie, augmentation anormale du taux d'urée dans le sang, est un autre de ces facteurs. Phénomène qui explique le nombre important de patients insuffisants rénaux concernés par ce problème.
Déambuler la nuit durant
"La plupart du temps, les patients qui présentent les symptômes du SJSR ont un sommeil très perturbé. Ils ont beaucoup de mal à s'endormir et ne peuvent s'empêcher de se relever pour faire disparaître les fourmillements qu'ils ressentent dans les jambes", explique le Pr Vandervelde. "Dans les cas les plus graves, le syndrome peut apparaître en soirée, lorsque les personnes sont assises. Il est donc très difficile pour elles d'aller au cinéma, de lire un livre ou de se rendre au restaurant." Invalidant à plus d'un titre, le SJSR ne peut être soigné. Reste donc à agir sur ses symptômes. "Réduire drastiquement sa consommation de tabac, d'alcool et de caféine permet déjà de réduire en partie l'inconfort", explique le Pr Vandervelde. "Faire des étirements ou des exercices physiques légers peut également soulager les patients." Si la prise de somnifères est fortement déconseillée, différents traitements médicamenteux peuvent être envisagés. "Les personnes les plus sensibles à cette pathologie sont ceux qui présentent des stocks en fer réduits. La première chose à faire consiste donc à leur fournir davantage de fer. Le traitement par érythropoïétine des patients dialysés peut également s'avérer efficace contre le SJSR", souligne le spécialiste. "Enfin, au cas où les symptômes persisteraient, des traitements plus lourds peuvent être proposés au patient tels que les agonistes de la dopamine, utilisés chez les patients parkinsoniens."
Parce que rien ne devrait nous empêcher de passer de douces nuits de repos...
Aurélie Bastin, avec la collaboration du Pr Dominique Vandervelde, chef du service de néphrologie des hôpitaux Iris Sud.
11. Cola et rein: une liaison dangereuse?
Contenant une quantité très importante de sucre (une canette équivaut à environ 6 sucres soit 150 kcal), le cola est loin d'être bénéfique pour la santé. Incriminé pour ses effets néfastes dans la prise de poids, le cola a également d'autres méfaits à son actif. Il a en effet été démontré il y a quelques années que les femmes qui boivent régulièrement du cola perdent entre 2,3 et 5 % de densité minérale osseuse. En cause: l'acide phosphorique (E338) présent dans ce type de boisson. Un tableau encore noirci par une nouvelle étude publiée dans la revue Epidemiology portant sur ses effets sur les reins.
Risque doublé d'insuffisance rénale
C'est en comparant la consommation de boissons de 465 patients atteints d'insuffisancerénale chronique à celle d'un groupe contrôle de 467 personnes en bonne santé qu'une équipe de chercheurs américains a pu mettre au jour l'influence néfaste du cola sur les reins. Conclusion: le risque de développer une insuffisance rénale chronique serait multiplié par 2 à partir de 2 verres par jour. Les consommateurs de boissons light ne seraient par ailleurs pas non plus épargnés. Si une canette de 33 cl de cola classique comporte de 44 à 62 mg d'acidephosphorique, la même quantité de boisson light en contient tout de même entre 27 et 39 mg.
Et les autres sodas?
Aucune association entre la consommation des autres boissons et l'insuffisancerénale chronique n'a pu être démontrée. Dans la mesure où la plupart d'entre elles contiennent de l'acide citrique plutôt que phosphorique, elles seraient sans danger pour les reins.
En attendant les résultats d'autres études en cours, il est vivement recommandé aux patients de consommer avec modération ce type de boisson, mais également les aliments riches en phosphore comme la viande, les fromages, les fruits secs ou encore les céréales.
Aurélie Bastin
Source: Saldana TM, Basso O et al. Carbonated beverages and chronic disease, Epidemiology, 2007, Jul; 18(4):501-6.
12. Comment rendre la dialyse plus agréable?

Pendant la dialyse, de nombreuses personnes dorment ou bavardent avec les autres patients ou le personnel infirmier. "L'hémodialyse est un traitement assez fatiguant", explique Johan De Troyer de vzw Nierpatiënten ASZ. "Sans compter que la liberté de mouvement est réduite durant les séances", ajoute Lut Buyle de vzw Nierpatiënten Dendermonde. Comment, dès lors, aménager ces moments pour les rendre les plus agréables possibles?
Lire et regarder la télévision durant la dialyse
Gino Matthys, membre de l'association Vriendenkring Nierpatiënten Roeselare passe quant à lui ses dialyses à bouquiner. Les journaux et les livres ont la cote durant les séances de dialyse. Certains hôpitaux proposent d’ailleurs un large choix de livres à leurs patients sous dialyse. "Des patients apportent leur pc portable", ajoute Gino Matthys. Dans certains centres de dialyse, il est même possible de surfer sur internet. Si votre emploi le permet, faire du télétravail à l'hôpital est donc aussi une possibilité. La plupart des hôpitaux mettent également à disposition une télévision et/ou un lecteur de DVD.
Peut-on manger et boire pendant la dialyse?
Autre distraction possible, grignoter un morceau et/ou siroter une boisson. Attention toutefois, manger et boire durant le traitement peut provoquer une chute de tension. Renseignez-vous auprès de votre centre de dialyse qui vous indiquera si vous pouvez vous restaurer et en quelle quantité.
Pédicure, massage et vélo durant le traitement
Dans certains hôpitaux, notamment à la Sint-Augustinusziekenhuis de Wilrijk et l’Algemeen Stedelijk Ziekenhuis d’Alost, il est possible de se faire faire une pédicure pendant la dialyse. Au CHU Brugmann à Bruxelles, les patients dialysés peuvent même se faire masser. Depuis quelques années, dans certains centres, il est également possible de faire du vélo pendant sa dialyse. A l’AZ Maria Middelares (AZMM) de Gand, par exemple, les personnes dialysées et le personnel infirmier parcourent chaque été leur propre Tour de France. Dans cet hôpital, les diététiciens animent aussi des séances d’information pendant la dialyse.
Du côté des associations de patients
Les associations de patients organisent elles aussi de nombreuses activités: la visite de Saint Nicolas, des petits cadeaux à Pâques et à Noël, une décoration saisonnière des unités de dialyse… Certaines associations planifient également chaque année un voyage à l’étranger et organisent des repas et autres événements pour le financer.
13. Cystinose: mieux la comprendre pour mieux la traiter
La cystinose est une maladie rare qui se caractérise par une accumulation de cystine (acide aminé) dans les tissus et les organes. "La cystine se forme au sein des cellules, dans une partie que l’on appelle le lysosome", explique le Dr Thierry Schurmans, chef de clinique adjoint à l’HUDERF (Hôpital Universitaire des Enfants Reine Fabiola) et spécialiste en néphrologie pédiatrique. "Lorsque tout fonctionne correctement, la cystine est évacuée des lysosomes grâce à un transporteur appelé cystinosine. Chez une personne atteinte de cystinose, la cystine s’accumule dans les tissus et perturbe le fonctionnement des reins."
Une maladie héréditaire
Il existe 3 formes de cystinose: la forme infantile, qui se manifeste chez les nourrissons, la forme juvénile et la forme adulte, plus rare et plus bénigne. La forme infantile est la plus fréquente. Elle représente aujourd’hui 1 naissance sur 200.000, ce qui correspond à 1 cas tous les 2 ans en Belgique. La cystinose est une maladie génétique liée à des mutations du gène de la cystinosine (CTNS). "Si les 2 parents sont porteurs d’un même gène défectueux, le bébé aura 1 chance sur 4 de naître avec la cystinose, qu'il s'agisse d'une fille ou d'un garçon. Lorsqu’il y a des antécédents connus dans la famille, nous proposons aux parents de faire un diagnostic prénatal pour détecter la maladie", précise le Dr Schurmans.
Comment reconnaître la cystinose?
Les premiers signes de la forme infantile de la maladie apparaissent chez les bébés âgés de 3 à 6 mois. Ils refusent de manger, vomissent facilement, boivent beaucoup, urinent beaucoup et souffrent d’importants retards de croissance. Le diagnostic se fait par le dosage de cystine dans les globules blancs du sang.
Un traitement efficace, mais contraignant
Sans traitement, la forme infantile évolue toujours vers une insuffisance rénale chronique terminale vers l’âge de 10 ans et finit par toucher d’autres organes: les yeux, la thyroïde, le pancréas ou le système nerveux central. Heureusement, une molécule, la cystéamine, permet d’éviter l’accumulation de cystine dans les cellules. Il faut la prendre à vie, à raison de 3 à 4 prises par jour avec idéalement une prise au milieu de la nuit. Il faut également y ajouter des gouttes pour les yeux à base de cystéamine. Elles doivent également être prises 4 à 6 fois par jour. Ce traitement permet de ralentir très fortement l’évolution de la maladie, voire d’éviter ses complications. Il donne malheureusement une odeur corporelle et une haleine très forte, ce qui est souvent difficile à vivre.
De nouvelles perspectives de traitement
"L’identification de la mutation du gène responsable de la maladie nous permet de mieux comprendre ses mécanismes. Aujourd’hui, nous espérons pouvoir trouver de nouvelles molécules avec la même efficacité que la cystéamine mais sans ses effets secondaires", précise le Dr Schurmans. D’ici quelques années, un médicament en une seule prise ou même un patch à diffusion continue sera peut-être disponible.
Stéphanie Paillet
14. Dépistage de l'insuffisance rénale

Diagnostic tardif de l'insuffisance rénale
Jusqu'à présent, l'insuffisance rénale n'était détectée que lorsque la maladie était déjà à un stade avancé de développement. L'apparition tardive des symptômes (fatigue excessive, hypertension...) et leur non-spécificité ne permettaient pas de soigner les patients au début de leur maladie, et encore moins d'intervenir de manière préventive. Une analyse de sang ou d'urine permettent de détecter des anomalies qui indiquent une fonction rénale défaillante, mais il est difficile d'anticiper l'apparition d'une insuffisance rénale.
Importance d'un diagnostic précoce
Le diagnostic précoce de l'insuffisance rénale est pourtant essentiel. Il permet en effet d'agir le plus efficacement possible sur les causes principales de la maladie que sont l'hypertension et le diabète et prévenir les complications (maladies cardiovasculaires, anémie, fragilité osseuse...).
Un outil de dépistage de l'insuffisance rénale
Une étude américaine récente a mis au point un nouvel outil de dépistage de l'insuffisance rénale. Pour ce faire, des prises de sang ont été effectuées sur plus de 2.300 participants présentant une fonction rénale normale. Dix ans plus tard, 17% d'entre eux souffraient d'insuffisance rénale chronique. Les chercheurs ont découvert que le sang de la plupart de ces patients contenait dès le départ une combinaison de trois molécules spécifiques:
- l'homocystéine (un acide aminé),
- l'aldostérone (une hormone impliquée dans la régulation de la pression artérielle),
- le peptide natriurétique B (une hormone secrétée par le coeur).
La présence de ces trois molécules indique que ces patients présentaient un risque important de développer une insuffisance rénale chronique. D'autres études sont toutefois nécessaires, notamment pour savoir s'il est possible de diminuer les risques de développer la maladie en agissant sur ces molécules.
15. Des pieds sous haute protection
En constante augmentation, le diabète touche aujourd’hui environ 5% de la population. Or, cette maladie, qui se caractérise par un excès de sucre dans le sang (en raison d’une action insuffisante de l’insuline), peut entraîner de nombreuses complications à long terme: atteinte des yeux, des vaisseaux… et des reins. Le diabète représente d’ailleurs actuellement la première cause d’insuffisancerénale.
Zone à risque
Une des complications les plus fréquentes chez le patient diabétique est l’infection des pieds, qui peut, si elle n’est pas prise en charge suffisamment tôt, déboucher sur une gangrène et une amputation. L’atteinte des vaisseaux chez le patient diabétique entraîne en effet souvent une mauvaise irrigation des membres inférieurs. Toutes les petites plaies se trouvant dans cette zone cicatriseront donc plus difficilement. De plus, en raison de l’atteinte des nerfs, le patient diabétique présente souvent une sensibilité amoindrie au niveau des pieds. De petites blessures sans importance peuvent ainsi s’infecter sans que le patient ne ressente de douleur ou de gêne. Le risque de voir dégénérer une petite lésion est donc élevé, a fortiori en cas d’insuffisancerénale chronique.
Les pieds à la loupe
Il est donc essentiel pour le patient d’examiner régulièrement ses pieds afin de prévenir l’infection de petites plaies. Durillons, gerçures, callosité, mycoses, ampoules… Chaque petite lésion devra être immédiatement traitée. Cette inspection doit se faire quotidiennement, si besoin à l’aide d’un petit miroir ou d’une autre personne. Si elles sont prises à temps, la grande majorité des lésions pourront être facilement traitées. À l'inverse, lorsqu’on laisse la plaie s’infecter, le risque de gangrène et d’amputation reste non négligeable.
Aux petits soins
Pour prévenir toute complication, il est impératif de procéder à un lavage quotidien des pieds à l’eau chaude en veillant à bien les sécher, surtout entre les orteils. Si la peau est sèche, talons et plantes des pieds devront être soigneusement hydratés. La coupe des ongles doit se faire à angles droits et être complétée par un limage délicat des coins. Pour cette étape, le recours à un podologue ou à un pédicure est souvent très utile. Par ailleurs, il est essentiel de posséder de bonnes chaussures et, si possible, de ne pas porter la même paire deux jours de suite afin d’éviter un phénomène de frottement régulier. Afin de minimiser le risque de blessure, il est également fortement déconseillé de marcher pieds nus chez soi.
Julie Luong
NEWS
 23 02 2011
23 02 2011
Insuffisance rénale
Un menu de Noël diététique et gastronomique
Entrée: noix de Saint-Jacques sur lit de chicons et pommes vertes au curry
Votre marché pour 4 personnes:
12 noix de Saint-Jacques fraîches
400 g de chicons
2 pom...
Lire la suite 23 02 2011
23 02 2011
Insuffisance rénale
Infections urinaires: quel impact sur les reins?
Très fréquentes – de 30 à 50% des femmes sexuellement actives auront au moins une infection urinaire dans leur vie – les cystites, mêmes récidivantes, ne sont que très ra...
Lire la suite 23 02 2011
23 02 2011
Insuffisance rénale
L'insuffisance rénale terminale: une maladie inflammatoire
Chez les patients souffrant d'insuffisancerénale terminale, les marqueurs de l'inflammation sont nettement augmentés, ainsi que le montrent les analyses de sang. Bien que...
Lire la suite 23 02 2011
23 02 2011
Insuffisance rénale
Vers une prise en charge totale des frais liés au don de rein
En 2009, plus de 95.500 personnes se sont enregistrées sur la liste des donneursd'organe, soit 62.500 de plus qu'en 2005. En nette augmentation, le nombre de donneurs ris...
Lire la suiteVIDEO
- «
- »
VOS ARTICLES PRÉFÉRÉS
SONDAGE
TÉMOIGNAGES
L'encadrement du patient dialysé: une priorité!

Tatiana Diakun, infirmière spécialisée dans la dialyse péritonéale
MALADIES À LA UNE
Alzheimer
Covid-19
Greffe d'organes
Leucémie myéloïde chronique
Migraine et maux de tête
Oeil infecté, irrité ou sec
Parkinson
Vessie hyperactive
PRÉVENTION À LA UNE
Toutes les thématiquesNEWSLETTER
NOS GUIDES
EN IMAGES
EN VIDEOS