Cancer du sein HER2 positif
Traitements
-
1. Comment traiter le cancer du sein HER2 positif?
2. La chimiothérapie avant chirurgie dans le cancer du sein
3. La chimiothérapie en association à un traitement ciblé
4. La radiothérapie dans le traitement du cancer du sein
5. Le pertuzumab: nouveau traitement ciblé anti-HER2
6. Le rôle de la chirurgie pour traiter le cancer du sein?
7. Le trastuzumab emtansine: nouveau traitement ciblé anti-HER2
8. Les traitements ciblés: le lapatinib (Tyverb®)
9. Les traitements ciblés: le trastuzumab (Herceptin®)
10. L’hormonothérapie dans le traitement du cancer du sein
11. Quel est le rôle des traitements ciblés du cancer du sein?
12. Zoom sur les nouveaux traitements anti-HER2
1. Comment traiter le cancer du sein HER2 positif?

Un plan de traitement adapté à ce type de cancer
La prise en charge du cancer du sein HER2 positif nécessite les mêmes traitements que pour tout cancer du sein. On fait appel aux traitements à action locale tels que la chirurgie et la radiothérapie. D’autres traitements, dits systémiques, complètent le plan de traitement: ce sont la chimiothérapie et l’hormonothérapie.
Mais pour le cancer HER2 positif, la séquence peut être différente et surtout un traitement ciblant le récepteur est ajouté aux traitements habituels du cancer du sein.
Réalisé avec la collaboration du Dr Joëlle Collignon.
2. La chimiothérapie avant chirurgie dans le cancer du sein
Parfois, la chimiothérapie est administrée avant la chirurgie: on l’appelle chimiothérapie néoadjuvante. Elle a pour but de réduire la taille de la tumeur et d’augmenter ainsi les chances de conservation du sein.
Dans le cas des cancers du sein HER2 positifs, ce traitement a d’autres implications. Il permet de commencer non seulement la chimiothérapie mais surtout le traitement ciblé sur les récepteurs HER2 plus tôt. Ce traitement augmente significativement le nombre de cas où il y aura une réponse pathologique complète. Cela signifie que la tumeur aura
disparu complètement lors de l’analyse histologique après la chirurgie. Ce résultat est atteint dans 40 à 60% des cas.
Réalisé avec la collaboration du Dr Joëlle Collignon.
3. La chimiothérapie en association à un traitement ciblé

Une place primordiale
Pour les cancers du sein HER2 positifs, la chimiothérapie en association avec un traitement ciblé occupe une place primordiale. Elle est proposée même pour des tumeurs de petite taille et de stade très précoce. Ce traitement est généralement administré sous forme de perfusion intraveineuse. Rappelons que ces traitements présentent des effets secondaires non négligeables contrairement aux traitements ciblés anti-HER2.
Avant ou après la chirurgie
La chimiothérapie peut débuter même avant la chirurgie, elle est dite néoadjuvante et permet, notamment, de réduire la taille de la tumeur. Elle peut également se donner après la chirurgie. Il s’agit alors d’un traitement adjuvant. Son rôle est d’éliminer de l’organisme les éventuelles cellules cancéreuses circulant dans le sang ou résiduelles pour augmenter les chances de guérison et diminuer le risque de récidive dans les années futures.
En cas de métastases
La chimiothérapie est aussi utilisée si le cancer revient sous forme de métastases et, dans ce cas, le but est de contrôler le cancer pour que la patiente vive plus longtemps avec la meilleure qualité de vie possible.
Exemples de chimiothérapie avec traitement ciblé
Le schéma le plus utilisé comprend une association d’anthracycline (adriamycine ou épirubicine) et de taxane (paclitaxel - Taxol® ou docétaxel - Taxotère®) en association avec le traitement ciblé. Ces deux chimiothérapies sont données de manière séquentielle (l’une après l’autre). Une évaluation cardiaque sera réalisée avant de débuter le traitement car les anthracyclines sont parfois toxiques pour le cœur. Cette toxicité n’est pas réversible et s’il y a déjà une atteinte au départ, un schéma alternatif sans anthracycline sera proposé comme une association de docétaxel et de carboplatine.
Réalisé avec la collaboration du Dr Joëlle Collignon.
4. La radiothérapie dans le traitement du cancer du sein
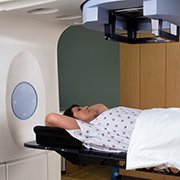
La radiothérapie complète le traitement locorégional du cancer du sein après la chirurgie. Sauf, dans certaines indications très limitées chez la femme de plus de 70 ans, elle est toujours proposée en cas de tumorectomie, c’est-à-dire d’enlèvement limité à la tumeur avec préservation du sein. Le but est de diminuer le risque de récidive locale. Ce traitement a aussi à long terme un effet sur la survie globale.
Par contre, en cas de mastectomie, c’est-à-dire d’enlèvement du sein, la radiothérapie a des indications plus limitées. Elle est proposée surtout en cas de tumeur de grande taille ou d’atteinte des ganglions. La présence éventuelle de plusieurs tumeurs dans le sein intervient également dans la décision. Le statut HER2 positif (ou pas) influence peu le choix de pratiquer une radiothérapie.
Réalisé avec la collaboration du Dr Joëlle Collignon.
5. Le pertuzumab: nouveau traitement ciblé anti-HER2

Mode d’action du pertuzumab (Perjeta®)
Cette molécule est un anticorps monoclonal comme le trastuzumab mais qui se lie à une autre partie du récepteur HER2. Son action est donc complémentaire au trastuzumab. Il se donne par voie intraveineuse toutes les 3 semaines.
Quand prendre le pertuzumab et pendant combien de temps?
Ce médicament est à présent accessible aux patientes qui ont développé des métastases et n’ont encore reçu aucun traitement (lors de la découverte des métastases). Il se donne en combinaison avec le trastuzumab et une chimiothérapie. Le traitement est poursuivi tant qu’il est efficace. Dans cette situation, l’association augmente de façon très significative la survie des patientes. Une étude internationale a testé son efficacité chez des patientes avec un cancer précoce (traitement adjuvant) mais les résultats ne sont pas encore connus.
Effets secondaires du pertuzumab
La toxicité cardiaque est possible comme pour le trastuzumab et nécessite la même surveillance. Mais donner ces deux anticorps en même temps n’augmente pas le risque d’endommager le cœur. Il peut aussi entraîner de la diarrhée ou une éruption cutanée ou encore des nausées et des douleurs abdominales. Le médecin surveillera via la prise de sang s’il n’y a pas de toxicité sur le foie.
Réalisé avec la collaboration du Dr Joëlle Collignon.
6. Le rôle de la chirurgie pour traiter le cancer du sein?

La chirurgie: le traitement de base du cancer du sein
La prise en charge chirurgicale est le traitement de base de tout cancer du sein. Elle consiste à enlever la tumeur:
- soit par une chirurgie conservatrice (tumorectomie) qui laisse en place le reste du sein;
- soit par une chirurgie complète de mastectomie qui enlève toute la glande mammaire. Le chirurgien enlèvera également les ganglions présents au niveau des aisselles: soit par la technique du ganglion sentinelle, soit par un curage axillaire complet quand la tumeur est de grande taille ou lorsqu’il y a plusieurs lésions dans le même sein.
Classification TNM de la tumeur
L’analyse de la pièce opératoire par l’anatomopathologiste permet de définir le stade de la tumeur selon la classification TNM.
- T pour tumor = taille de la tumeur et présence d’une éventuelle extension à la peau ou à la paroi de la cage thoracique
- N pour nodes = nombre de ganglions envahis
- M pour metastases = propagation à un autre organe
Réalisé avec la collaboration du Dr Joëlle Collignon.
7. Le trastuzumab emtansine: nouveau traitement ciblé anti-HER2
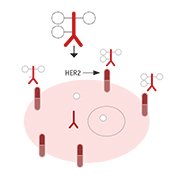
Mode d’action du trastuzumab emtansine ou T-DM1 (Kadcyla®)
Le trastuzumab emtansine ou T-DM1 est un anticorps monoclonal conjugué. Le trastuzumab est lié à une chimiothérapie très efficace, un dérivé de la maytansine (DM1), mais toxique si elle est administrée seule. Ce composé permet d’amener directement dans la cellule tumorale la chimiothérapie qui peut alors agir spécifiquement sur la tumeur. C’est un «bonbon empoisonné» pour la cellule tumorale. L’efficacité est augmentée et les effets secondaires diminués. Il représente une nouvelle révolution dans le traitement des cancers du sein HER2 positifs.
Mode d’administration du T-DM1
Le T-DM1 est un anticorps conjugué administré en perfusion intraveineuse toutes les 3 semaines. La durée de la perfusion est de 90 minutes la première fois puis 30 minutes.
Quand prendre le T-DM1 et pendant combien de temps?
Il sera accessible aux patientes souffrant d’un cancer du sein métastatique qui évolue après un premier traitement par chimiothérapie et trastuzumab. Il sera alors donné tant qu’il est efficace c’est-à-dire tant que la maladie ne progresse pas. Il sera arrêté plus tôt si la toxicité est trop importante. Des études sont en cours pour évaluer ce traitement dans les cancers du sein HER2 positifs au stade précoce, avant et après chirurgie (en néoadjuvant et en adjuvant).
Effets secondaires du T-DM1
La particularité de ce traitement est sa faible toxicité par rapport à une chimiothérapie classique. Comme pour le trastuzumab, la surveillance cardiaque est importante. On observe également des réactions lors de la perfusion mais ces effets sont rarement sévères. Des prises de sang régulières s’imposent car le T-DM1 peut faire chuter les plaquettes et altérer le fonctionnement du foie. Enfin, on a rarement décrit une toxicité sur les nerfs périphériques (des membres) entraînant des picotements ou une diminution de la sensibilité des doigts et des orteils.
Réalisé avec la collaboration du Dr Joëlle Collignon.
8. Les traitements ciblés: le lapatinib (Tyverb®)

Mode d’administration du lapatinib
Le lapatinib est un inhibiteur de tyrosine kinase. Il agit sur le récepteur HER2 mais aussi HER1, ce qui explique qu’il peut donner un peu plus d’effets secondaires. Il s’administre par voie orale tous les jours: 5 ou 6 comprimés de 250 mg sont pris en une seule fois 1 heure avant ou 1 heure après le repas. Il n’est pas permis de répartir la dose sur la journée.
Quand prendre le lapatinib et pendant combien de temps?
Actuellement, ce traitement n’est utilisé que dans les cancers du sein HER2 positif à un stade avancé, avec métastases. Ce traitement est poursuivi tant qu’il est efficace ou qu’il ne donne pas d’effets secondaires trop importants.
Effets secondaires du lapatinib
- Effets secondaires sur le cœur
Il existe un risque de toxicité cardiaque. Une surveillance par échographie est aussi nécessaire.
- Effets secondaires sur le foie
Ce traitement peut être toxique pour le foie et votre médecin surveillera la prise de sang. Vous devez le contacter si vos urines sont foncées ou si vos yeux sont jaunes.
- La diarrhée
La diarrhée est aussi un effet secondaire fréquent et parfois sévère nécessitant l’arrêt transitoire du traitement. En cas de diarrhée, il faut bien s’hydrater et suivre les conseils de votre médecin.
- Effets secondaires sur la peau
La peau peut aussi être affectée par des rougeurs ou des boutons qui sont parfois traités par antibiotique.
- Autres effets secondaires
Des nausées, de la fatigue et des rougeurs des mains et des pieds appelées «syndrome mains/pieds», plus fréquentes avec l’association à la capécitabine (Xeloda® ) peuvent également survenir. Et très rarement, le poumon peut être touché mais cette atteinte est réversible à l’arrêt du traitement. Vous devez contacter votre médecin si vous toussez ou si vous êtes essoufflée.
Réalisé avec la collaboration du Dr Joëlle Collignon.
9. Les traitements ciblés: le trastuzumab (Herceptin®)
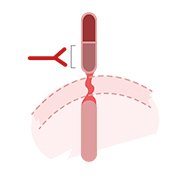
De très bons résultats contre le cancer du sein HER2 positif
Le trastuzumab (Herceptin®) a révolutionné le traitement du cancer du sein HER2 positif. Ce sous-type de cancer HER2 décrit dans les années 80 avait mauvaise réputation vu son agressivité. Mais très rapidement, le pronostic s’est amélioré grâce au développement des traitements ciblés. Après d’excellents résultats en situation métastatique, l'Herceptin® a amélioré la survie des patientes avec un cancer en stade précoce. Les études auxquelles ont participé plus de 13.000 patientes ont montré que l’ajout d’Herceptin® à la chimiothérapie standard diminuait le risque de rechute de 40%. En oncologie, il n’y a actuellement aucun autre anticorps monoclonal qui a donné de tels résultats.
Mode d’administration du trastuzumab
Le trastuzumab est un anticorps monoclonal qui vise spécifiquement le récepteur HER2. Il s’administre en perfusion par voie intraveineuse (IV) ou en administration sous-cutanée (SC).
Le traitement par trastuzumab IV débute par une dose de charge qui se donne en 90 minutes. Les doses ultérieures sont données en 30 minutes.
Le trastuzumab en administration sous-cutanée, c’est-à-dire injecté sous la peau, a été développé récemment. Cette méthode d’administration très aisée et rapide (2 à 5 minutes), ne nécessite pas de dose de charge et atteint une efficacité et une sécurité comparables à la forme IV. Cette forme est disponible dans la pratique quotidienne en Belgique.
Quand prendre le trastuzumab et pendant combien de temps?
Pour le traitement adjuvant du cancer du sein HER2 positif, le trastuzumab est donné durant 18 cycles toutes les 3 semaines. De cette manière, les chances de guérison ainsi que les chances d’éviter les rechutes sont optimisées. Le bénéfice est aussi supérieur si le traitement ciblé est débuté en même temps (traitement concomitant) que la chimiothérapie plutôt qu’après (séquentiel).
Dans certaines situations, le trastuzumab, en association avec la chimiothérapie, est administré avant la chirurgie. Dans ce cas, le trastuzumab est ensuite poursuivi seul après le traitement chirurgical pour atteindre la durée requise de 18 cycles.
Si le cancer du sein est à un stade plus avancé, le trastuzumab est aussi utilisé en association avec d’autres traitements à différents moments de la progression de la maladie. Dans ce cas, le traitement est poursuivi tant qu’il est efficace et qu’aucune progression ne survient. Il augmente le temps sans progression du cancer et la survie de la patiente.
Effets secondaires du trastuzumab
- Effets secondaires sur le cœur
Le principal effet secondaire est le risque de toxicité cardiaque. Un bilan cardiaque est toujours réalisé avant le début du traitement: échographie ou scintigraphie cardiaque. Ensuite, une évaluation tous les 3 mois est requise pendant toute la durée du traitement et même après. Si on observe une diminution de la fonction cardiaque, le traitement est interrompu. Comme la toxicité est réversible, le trastuzumab pourra être repris si la fonction cardiaque récupère. Dans tous les cas, vous devez contacter le médecin si vous respirez moins bien, si vous êtes essoufflée ou si vos pieds sont gonflés.
- Fièvre et frissons
Pendant la perfusion, il y a parfois des effets secondaires tels que de la fièvre et des frissons. La perfusion est alors interrompue puis reprise lorsque ces symptômes ont disparu. Il est rare que ces effets soient importants mais des réactions allergiques sévères peuvent parfois conduire à un arrêt définitif du traitement. Enfin, les effets secondaires les plus fréquents sont des symptômes grippaux avec fièvre, toux, maux de tête, douleurs musculaires et fatigue mais ils sont peu importants et altèrent rarement la qualité de vie.
Réalisé avec la collaboration du Dr Joëlle Collignon.
10. L’hormonothérapie dans le traitement du cancer du sein

Traitements hormonaux: dans quels cas?
L’hormonothérapie est toujours prescrite si la tumeur présente des récepteurs hormonaux aux œstrogènes et/ou à la progestérone, ce qui est le cas dans 50% des cancers du sein HER2 positifs. Ces traitements hormonaux ont pour objectif de bloquer l’activité de ces récepteurs ou de réduire la production hormonale. Différents traitements hormonaux existent et sont donnés par voie orale pendant plusieurs années.
Inhibiteurs des récepteurs aux hormones (Tamoxifène - Nolvadex®)
Ils se fixent aux récepteurs hormonaux et empêchent leur fonctionnement.
Inhibiteurs de l’aromatase
Ils bloquent la production des hormones féminines dans les glandes surrénales et le tissu graisseux. Les inhibiteurs de l’aromatase n’agissent pas sur la production par les ovaires et sont donc réservés à la femme ménopausée. Il s’agit de l’anastrozole (Arimidex®), de l’exémestane (Aromasin®) ou du létrozole (Femara®).
Suppression de la production hormonale au niveau des ovaires
La suppression de la production hormonale est possible:
- soit par voie chirurgicale en enlevant les ovaires (ovariectomie);
- soit en inhibant la fonction des ovaires avec des injections mensuelles d’analogues de la gonadolibérine (Zoladex®).
HER2 positives: des tumeurs plus résistantes
Les cancers du sein HER2 positifs ont tendance à être plus résistants au traitement hormonal. Le traitement par inhibiteurs de l’aromatase est le plus actif en cas de cancer du sein HER2 positif chez la femme ménopausée. Ces traitements en association avec des analogues de la gonadolibérine sont toujours à l’étude chez la femme non ménopausée.
Réalisé avec la collaboration du Dr Joëlle Collignon.
11. Quel est le rôle des traitements ciblés du cancer du sein?
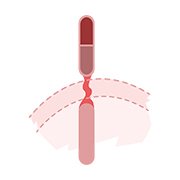
Cibler les cellules cancéreuses
Certains cancers du sein présentent des cibles particulières peu présentes sur les cellules normales. On peut donc viser les cellules tumorales sans être trop toxique pour les cellules normales. On parle alors de thérapie ciblée. Le plus ancien et le plus bel exemple de traitement ciblé est le traitement antihormonal par tamoxifène. Ce médicament a pour cible les récepteurs hormonaux présents sur les cellules du cancer du sein dans 60% des cas.
Deux grandes classes de traitements ciblés
Ces traitements sont dirigés sur une cible qui peut être, par exemple, une partie du récepteur HER2. Parfois, la cible est une protéine présente au sein même de la cellule et pas à la surface de celle-ci. C’est le cas dans le traitement de la leucémie myéloïde chronique dont la prise en charge a été fortement améliorée dans les années 90 comme pour le cancer du sein HER2 positif. Deux grandes classes de traitements ciblés ont été développées. D’une part, les anticorps monoclonaux et d’autre part, les inhibiteurs de tyrosine kinase.
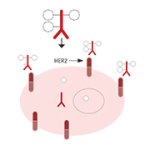
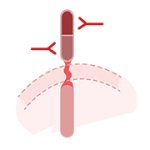
Les anticorps monoclonaux
Les globules blancs produisent des anticorps, des protéines produites par le système immunitaire qui protègent l’organisme contre les intrusions (infection, cancer...). Sur cette base, des chercheurs ont développé en laboratoire des anticorps contre des cibles spécifiques à certaines cellules cancéreuses. Ce sont les anticorps monoclonaux. L’identification de ces cibles a changé la stratégie thérapeutique des médecins: ces traitements sont efficaces uniquement chez les patients dont la tumeur présente la cible visée.
Par ailleurs, ces traitements ciblés ont des effets secondaires réduits par rapport aux traitements comme la chimiothérapie. Ces anticorps s’administrent sous forme de perfusion toutes les 2 ou 3 semaines.
Les inhibiteurs de tyrosine kinase
Dans certains cas, comme pour le récepteur HER2, une partie intracellulaire (située dans la cellule) du récepteur visé contient une enzyme appelée «protéine kinase» qui intervient aussi dans la prolifération de la cellule et la stimule à se diviser de manière incontrôlable. Les médicaments ciblant cette protéine sont appelés inhibiteurs de tyrosine kinase. Il s’agit de petites molécules qui se donnent par voie orale, tous les jours.
Réalisé avec la collaboration du Dr Joëlle Collignon.
12. Zoom sur les nouveaux traitements anti-HER2

L’Herceptin® a fortement amélioré le pronostic du cancer du sein HER2 positif. Mais de nouvelles molécules très actives sont aussi disponibles pour encore augmenter l’efficacité du traitement de ce type de cancer du sein. La participation des patientes aux études cliniques a permis le développement des molécules comme le pertuzumab, le trastuzumab emtansine (ou TDM-1) et l’évérolimus. Ces études sont primordiales pour continuer à progresser dans cette voie. On montre l’efficacité du médicament d’abord à un stade avancé de la maladie. Il est ensuite testé pour un cancer localisé avec comme but d’augmenter les chances de guérison définitive et la survie des patientes.
Réalisé avec la collaboration du Dr Joëlle Collignon.
NEWS
 03 12 2024
03 12 2024
Cancer du poumon
L'IA: une solution pour le diagnostic du cancer
La distinction entre un kyste bénin et une tumeur maligne n’est pas toujours évidente: sur une image CT (rayons X), kystes et tumeurs peuvent sembler très similaires. Cet...
Lire la suite 10 11 2015
10 11 2015
Cancer du sein HER2 positif
Un traitement adapté au cancer du sein précoce
Les résultats d’une nouvelle étude scientifique constituent une avancée dans l’élaboration d’un traitement adapté au stade précoce du cancer du sein HER 2 positif.
A...
Lire la suite 29 09 2015
29 09 2015
Cancer du sein HER2 positif
Cancer du sein: chirurgie ou radiothérapie des ganglions?
Dans le cancer du sein, les cellules cancéreuses peuvent se propager dans le corps via le sang ou la lymphe, un liquide qui circule à travers les vaisseaux lymphatiques e...
Lire la suite 14 09 2015
14 09 2015
Cancer du sein HER2 positif
Cancer du sein: une hausse des mastectomies
Selon une récente étude, de plus en plus de patientes atteintes d’un cancer du sein préfèreraient la mastectomie, c’est-à-dire l’ablation complète du sein, à la chiru...
Lire la suite- «
- »
VOS ARTICLES PRÉFÉRÉS
 25 10 2022
25 10 2022
Cancer du sein
Un vaccin contre le cancer d'ici 2030?
VRTNWS s'est rendu à la Journée contre le cancer pour jeter un coup d'œil à l'hôpital universitaire d'Anvers, qui travaille assidûment à une avancée : «C'est prometteur,...
Lire la suiteSONDAGE
TÉMOIGNAGES
Cancer du sein HER2+: quel impact sur la vie familiale?

Dr Corina Martinez-Mena, oncologue médical à la Clinique du sein ISALA du CHU Saint-Pierre.
Cancer du sein HER2 positif: quel impact sur le travail?

Pr Hannelore Denys, chef de clinique d’oncologie UZ Gent
MALADIES À LA UNE
Alzheimer
Covid-19
Greffe d'organes
Leucémie myéloïde chronique
Migraine et maux de tête
Oeil infecté, irrité ou sec
Parkinson
Vessie hyperactive
PRÉVENTION À LA UNE
Toutes les thématiquesNEWSLETTER
MALADIES LIÉES
Cancer du seinEN IMAGES